Lebende Augentropfen? Gentechnisch veränderte Bakterien fördern Hornhautheilung
Forscher der University of Pittsburgh haben ein neuartiges Konzept für die Therapie von Hornhautverletzungen entwickelt: genetisch modifizierte Augenbakterien, die entzündungshemmendes Interleukin-10 freisetzen. In einem Mausmodell beschleunigte der Ansatz die Heilung des Hornhautepithels und könnte langfristig neue Möglichkeiten für die Behandlung von Erkrankungen der Augenoberfläche eröffnen.
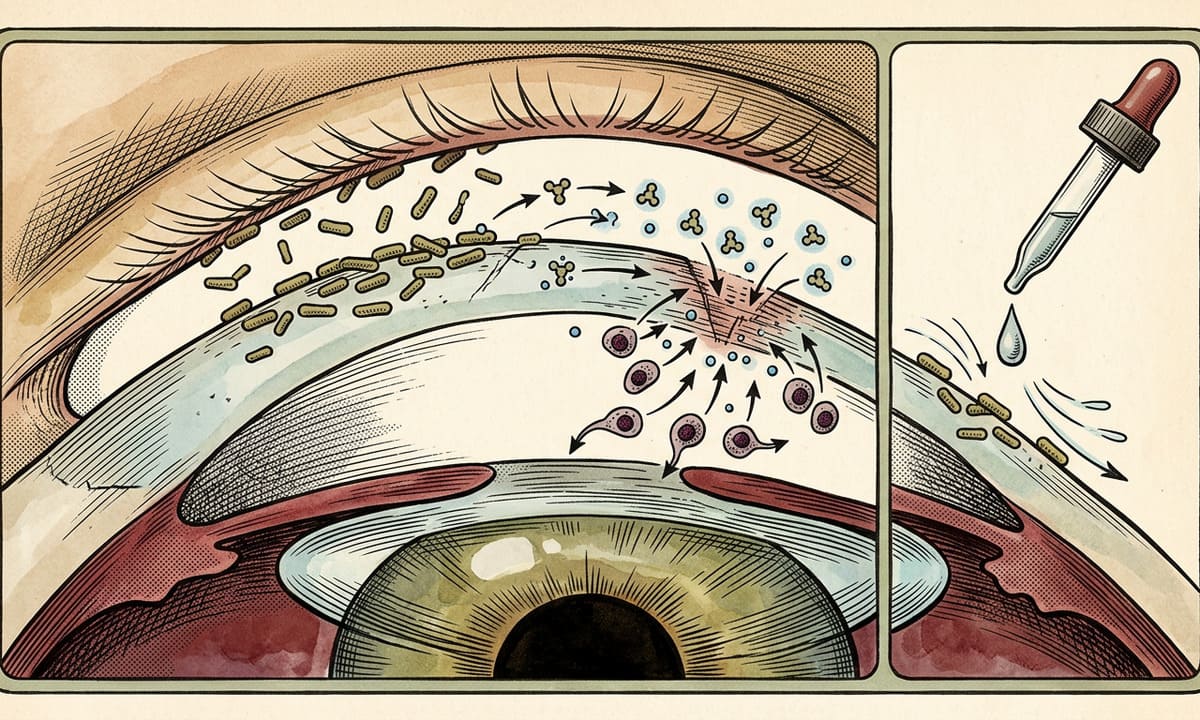
Die in Cell Reports veröffentlichte Proof-of-Concept-Studie zeigt, dass das auf der Cornea vorkommende, apathogene Stäbchenbakterium Corynebacterium mastitidis genetisch so verändert werden kann, dass es ein entzündungshemmendes Therapeutikum absondert, das im Mausmodell die Heilung nach einer Hornhautverletzung fördert.
„Dies ist der erste Nachweis, dass ein auf der Augenoberfläche lebender Mikroorganismus so verändert werden kann, dass er ein Therapeutikum freisetzt, das die Augengesundheit verbessert“, sagte der leitende Autor Anthony St. Leger, außerordentlicher Professor für Augenheilkunde und Immunologie am UPMC Vision Institute. „Dies öffnet die Tür für die Idee einer ‚lebenden Medizin‘ für das Auge – eine Therapie, die einmal appliziert wird, anschließend auf der Augenoberfläche verbleibt, das Gewebe schützt und dessen Heilung unterstützt.“
Da Tränen topisch applizierte Medikamente kontinuierlich verdünnen und abspülen, erfordert die Behandlung von Erkrankungen der Augenoberfläche häufig die mehrfache tägliche Applikation von Augentropfen. Dies kann die Wirksamkeit von Therapien bei Erkrankungen wie Hornhauterosionen oder Sicca-Syndrom einschränken.
Um eine alternative Applikationsstrategie zu untersuchen, modifizierte das Team der Universität Pittsburgh C. mastitidis – ein gutartiges Bakterium, das natürlicherweise unter dem Augenlid vorkommt – genetisch so, dass es kontinuierlich das Zytokin Interleukin-10 (IL-10) absondert, ein kleines Protein, das entzündungshemmende und immunregulatorische Effekte vermittelt.
Bei Mäusen heilten experimentell induzierte Hornhautläsionen, die mit den gentechnisch veränderten Bakterien behandelt wurden, schneller als solche, die mit Wildtyp-Bakterien oder Kochsalzlösung behandelt wurden. Wurde der IL-10-Rezeptor blockiert, verschwand dieser Effekt, was bestätigt, dass die therapeutische Wirkung IL-10-abhängig war.
Die Forscher entwickelten zudem eine Variante des Bakteriums, die humanes IL-10 freisetzt. In vitro verbesserte dies den Wundverschluss in kultivierten humanen Hornhautepithelzellen und reduzierte entzündliche Signalwege in menschlichen Immunzellen. Diese Ergebnisse liefern erste Hinweise darauf, dass der Ansatz prinzipiell auch für eine klinische Anwendung beim Menschen adaptierbar sein könnte, auch wenn noch erhebliche Entwicklungsarbeit erforderlich ist.
„Das Spannende an diesem System ist sein modularer Aufbau“, erklärte St. Leger. „Wir haben es so konzipiert, dass sich verschiedene Gene – etwa für Zytokine, Wachstumsfaktoren oder andere therapeutische Proteine – austauschen lassen, um die Therapie gezielt an bestimmte Augenerkrankungen anzupassen.“
Trotz der vielversprechenden Ergebnisse befindet sich die Technologie noch in einem frühen Entwicklungsstadium. Die Autoren betonen, dass vor einer möglichen klinischen Anwendung zahlreiche weitere Schritte erforderlich sind. Dazu gehört unter anderem die Entwicklung integrierter „Kill-Switch“-Mechanismen, mit denen sich die manipulierten Bakterien bei Bedarf sicher deaktivieren oder eliminieren lassen.
Erkrankungen wie schweres trockenes Auge, entzündliche Erkrankungen der Augenoberfläche und traumatische Hornhautverletzungen betreffen jährlich Millionen von Menschen. Die Studie stellt zwar noch keine klinisch anwendbare Therapie dar, liefert jedoch eine Grundlage für die weitere Untersuchung, ob synthetisch entwickelte lebende Biotherapeutika künftig eine langfristige Freisetzung entzündungshemmender oder regenerativer Moleküle auf der Augenoberfläche ermöglichen könnten.
„In meinem Labor entwickeln wir normalerweise keine völlig neuen Therapieansätze“, fügte St. Leger hinzu. „Eine messbare Verbesserung der Heilung in einem Tiermodell zu sehen, basierend auf einem von uns entwickelten System, war äußerst motivierend und eröffnet spannende Perspektiven für zukünftige Forschungsarbeiten.“
Quelle: University of Pittsburgh
Originalarbeit: Jackie Shane, Matthew Evans, Yannis Rigas, Robert M.Q. Shanks, Anthony J. St. Leger, Genetically engineered eye-colonizing microbes that deliver the anti-inflammatory cytokine interleukin-10 enhance corneal tissue repair, Cell Reports2026, https://doi.org/10.1016/j.celrep.2026.117064.