Stammzell-basierte Retinaimplantate: Forschungsprojekt „KryoRet“ erfolgreich abgeschlossen
Forschern der Fraunhofer-Institute IBMT, ISC, IST und dem Fraunhofer TLZ-RT ist es gelungen, zusammen mit international renommierten Spezialisten der Augenklinik Sulzbach/Saar neuartige Methoden zur klinischen Translation von Stammzell-basierten Retinaimplantaten zur Heilung von z. B. altersabhängiger Makuladegeneration (AMD) zu erarbeiten.

Die steigende Anzahl an klinischen Studien von humanen induzierten pluripotenten Stammzellen (hiPSC) in der Ophthalmologie verlangt dringend nach neuen Methoden des Tissue Engineerings, der Langzeitlagerung und Logistik, um eine Unabhängigkeit vom Spendermaterial zu erreichen und funktionale Implantate zum Patienten zu bringen.
Finanziell konkurrenzfähiges Behandlungskonzept
Neuartige, regenerative Therapieformen stehen bei der AMD am Beginn der klinischen Erprobung. Diese beruhen auch auf dem Ersatz des erkrankten Gewebes durch Stammzell-basierte, flächige Implantate von retinalem Pigmentepithel (RPE) hinter die Netzhaut. Eine derartige regenerative Behandlung hat bei rechtzeitiger Anwendung das Potenzial zur Heilung der AMD. Dies wäre für den Großteil der betroffenen Patienten ohne aktuelle Behandlungsmöglichkeit ein enormer Gewinn an Lebensqualität. Langfristig wäre dies für das Gesundheitssystem, auch hinsichtlich einer möglichen Ablösung der IVOM-Therapie, ein finanziell konkurrenzfähiges Behandlungskonzept. Da die AMD nicht zuletzt auch auf multifaktorieller genetischer Veranlagung beruht, sind zur Gewinnung der Ausgangszellen passende Fremdspenden erforderlich. Zudem schließt sich das Zeitfenster zur erfolgreichen Therapie schnell, da der Aufbau eines implantationsfertigen Gewebes etwa zwei Monate dauert. Daher ist eine effiziente Bevorratung von funktionalen Implantaten für eine breite klinische Nutzung des Verfahrens notwendig.
Interdisziplinäre Zusammenarbeit eröffnet neue Möglichkeiten für AMD-Therapie
Das Fraunhofer-MAVO-Projekt „KryoRet“ zielte auf die Schaffung der technischen und biotechnologischen Voraussetzungen für eine Lagerhaltung eines hiPSC-basierten RPE Implantats ab. Um dieses Gesamtziel zu erreichen, arbeiteten die beteiligten Fraunhofer-Institute für Biomedizinische Technik IBMT, für Silicatforschung ISC, für Schicht- und Oberflächentechnik IST und das Fraunhofer-Translationszentrum für Regenerative Therapien TLZ-RT mit komplementären Expertisen interdisziplinär zusammen, immer in engem fachlichen Austausch mit den Chirurgen der Augenklinik Sulzbach, um die komplexen Aspekte der klinischen Anwendung zu berücksichtigen. Um die ambitionierten Ziele in Hinblick auf Aspekte der Materialwissenschaft, Oberflächenfunktionalisierung, partikulärer Formulierung sowie Stammzell- und Kryotechnologie zu erreichen, wurden in diesem Gemeinschaftsprojekt die Kompetenzen der Fraunhofer-Institute ISC, IST und IBMT gebündelt.
Maßgeschneiderte Trägermembran
Mittels einer im Labor hergestellten maßgeschneiderten Trägermembran, wurde dem Implantat eine physiologische und funktionale Gerüststruktur verliehen. Hierbei wurde eine poröse Membran aus ORMOCER® mit SiO2-Fasern kombiniert, um geeignete Diffusionseigenschaften, Zellinteraktion sowie Lagerstabilität zu erreichen. Die Stammzell-Technologie findet derzeit insbesondere im Bereich der Ophthalmologie in internationalen klinischen Studien („first-in-man“) große Beachtung, da sie ein vielversprechendes Werkzeug darstellt, um zukünftig Eigen- und Fremdimplantate herstellen zu können. Im Projekt wurden daher auch Differenzierungsprotokolle für retinale Pigmentepithelzellen etabliert, um die Funktionalität der Konstrukte direkt mit hiPSC-abgeleiteten RPE zu validieren. Da die Herstellungsdauer mehr als 60 Tage betrug, sind Lagerungstechnologien unabdingbar.
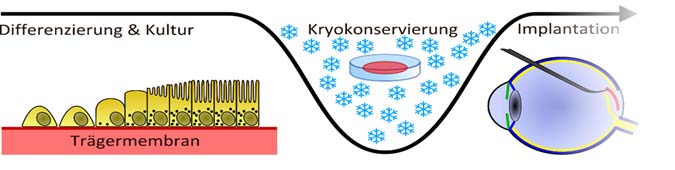
Bild: Fraunhofer-Institute für Biomedizinische Technik IBMT
Implantate kontrolliert einfrieren, lagern und dabei die Qualität sichern
Um das künstliche RPE zu kultivieren, entwickelte das Forscherteam einen Demonstrator für den Lagerbehälter sowie ein Einfrierprotokoll, wodurch das Implantat über passiv kontrolliertes Eiswachstum vor schädlichen Konzentrationsgradienten geschützt werden kann. Zugleich dient der Behälter zur Kultivierung der Implantate. Im Projekt „KryoRet“ wurden darüber hinaus Assays zur Bewertung der entwickelten Technologien etabliert. Es ist wichtig, dass diese keinen irreversiblen Einfluss auf die Implantate ausüben, sodass das Implantat selbst auf Funktionalität getestet und anschließend implantiert werden kann. Anhand von Mikroskopaufnahmen wurde beispielsweise ein Testdatensatz für maschinelles Lernen auf die verschiedenen Stadien der RPE-Kulturen während der Differenzierung erstellt, um zukünftig eine automatisierte Qualitätskontrolle durchzuführen.
Experteneinschätzung: Großes Potenzial des Lösungsansatzes
Während der gesamten Laufzeit wurde das Projekt von Experten der Augenklinik Sulzbach (Knappschaftsklinikum Saar) begleitet. Dadurch wurden bei der Entwicklung der Demonstratoren klinische Anforderungen frühzeitig berücksichtigt, um die spätere klinische Translation zu vereinfachen. „Durch die Ergebnisse des Projekts „KryoRet“ wurde ein bislang fehlender translationaler Grundstein gelegt, um den Forschungsstandort Deutschland für Zulassungsarbeiten von Zelltherapeutika bei AMD attraktiv zu machen", meint PD Dr. med. Boris Stanzel, Leiter des Makulazentrums und des Klinischen Studienzentrums der Augenklinik Sulzbach.
Quelle: Fraunhofer-Institute für Biomedizinische Technik IBMT